Идет формирование бланка результата. Через несколько секунд он появится в загрузках вашего браузера.
Просмотр результатов
Калькулятор пересчёта единиц измерения
Анализы и цены
О Гемохелп
Адреса отделений
Акции
Программа лояльности
Вакансии
Версия для слабовидящих
Политика обработки персональных данных Справка для ФНС Телефоны вышестоящих организаций Программа государственных гарантий
Как сдать анализы и сделать дозаказ Сроки выполнения и получения результатов Вызов на дом Пересчёт единиц измерения
Политика обработки персональных данных Справка для ФНС Телефоны вышестоящих организаций Программа государственных гарантий
Как сдать анализы и сделать дозаказ Сроки выполнения и получения результатов Вызов на дом Пересчёт единиц измерения
Вернуться
- Срочные анализы
- Комплексные исследования
- Гематологические исследования
- Биохимические исследования
- Опухолевые маркеры
- Микроэлементы, витамины, аминокислоты
-
Иммунологические исследования
- Иммунный статус
-
Маркеры аутоиммунных заболеваний
- Диагностика аутоиммунного заболевания щитовидной железы
- Диагностика антифосфолипидного синдрома
- Диагностика системных заболеваний соединительной ткани
- Ревматоидный артрит, заболевания суставов
- Диагностика аутоиммунного поражения печени
- Васкулиты и поражения почек
- Диагностика аутоиммунного поражения желудочно-кишечного тракта
- Диагностика аутоиммунного заболевания кожи
- Диагностика заболевания сердца
- Проблемы репродуктивной системы
- Диагностика аутоиммунного заболевания поджелудочной железы
- Диагностика неврологических заболеваний
-
Диагностика аллергии
- Специфические IgE к пищевым аллергенам
- Специфические IgE к смеси аллергенов
- Специфические IgE к аллергенам пыльцы деревьев
- Специфические IgE к аллергенам сорных и луговых трав
- Специфические IgE к бытовым аллергенам
- Специфические IgE к эпидермальным аллергенам и белкам животного происхождения
- Специфические IgE к лекарственным аллергенам
- Специфические IgE к контактным аллергенам
- Специфические IgE к инсектным аллергенам
- Рекомбинантные аллергены
- Пищевая непереносимость
-
Гормональные исследования
- Лабораторная оценка функции щитовидной железы
- Лабораторная оценка состояния репродуктивной системы и мониторинг беременности
- Лабораторная оценка эндокринной функции почек и надпочечников
- Биогенные амины
- Лабораторная оценка эндокринной функции поджелудочной железы
- Гормон жировой ткани
- Эритропоэз
- Костный метаболизм
- Гормоны роста
- Функция эпифиза
- Оценка состояния желудочно-кишечного тракта
-
Диагностика инфекционных заболеваний
-
Вирусные инфекции
- Аденовирус, Ротавирус, Норовирус, Астровирус
- Варицелла-Зостер вирус (ветряная оспа, опоясывающий лишай)
- ВИЧ
- Герпес
- Гепатит А
- Гепатит В
- Гепатит Е
- Гепатит С
- Гепатит D
- Гепатит G
- Гепатит ТТV
- Грипп
- ОРВИ
- Коронавирус (COVID-19)
- Клещевой энцефалит
- Корь
- Краснуха
- Папилломавирусная инфекция
- Паротит эпидемический
- Респираторно-синцитиальный вирус
- Цитомегаловирус
- Энтеровирус
- Эпштейна-Барр вирус
-
Бактериальные инфекции
- Эрлихиоз, Анаплазмоз
- Дисбиотические состояния кишечника и урогенитального тракта
- Боррелиоз (болезнь Лайма)
- Бруцеллез
- Гарднерелла
- Гонорея
- Дифтерия
- Иерсиниоз
- Клостридиоз
- Коклюш, Паракоклюш, Бронхисептикоз
- Листериоз
- Микоплазменная инфекция
- Сальмонелла
- Сифилис
- Столбняк
- Стрептококковая инфекция
- Туберкулез
- Уреаплазменная инфекция
- Хеликобактерная инфекция
- Хламидийная инфекция
- Энтеробактерии, кампилобактерии
- Исследование на простейшие, паразиты, грибы
-
Вирусные инфекции
- Исследование кала
- Исследование мочи
- Цитологические исследования
- Гистологические исследования
- Бактериологические исследования
- Общие микроскопические исследования
-
Молекулярно - генетические исследования
- HLA-типирование генов
- Гематология
-
Моногенные заболевания
- Адреногенитальный синдром
- Акродерматит энтеропатический
- Альбинизм
- Анемия Даймонда-Блекфена
- Атрофия зрительного нерва
- Аутоиммунный лимфопролиферативный синдром
- Боковой амиотрофический склероз
- Велокардиофациальный синдром
- Вильсона-Коновалова болезнь
- Гемофилия
- Дефицит гормона гипофиза, комбинированный
- Миотония Томсена/Беккера
- Миотоническая дистрофия
- Муковисцидоз
- Мышечная дистрофия
- Нефротический синдром
- Остеопороз рецессивный (мраморная болезнь костей)
- Ретта синдром
- Фенилкетонурия
- Хорея Гентингтона (Болезнь Хангтингтона)
- Цистиноз нефропатический
- Эритрокератодермия
- Эритроцитоз рецессивный
- Риск развития онкологических заболеваний
- Определение биологического родства
- Носительство частых мутаций для наиболее частых наследственных заболеваний
- Бесплодие и невынашивание беременности, риск патологии плода
- Мультифакторные состояния
- Идентификация личности по ДНК
- Выделение ДНК из нестандартного образца
- Выделение ДНК при повторном предоставлении образца
- Судебная / досудебная экспертиза
- Комплексные генетические исследования
- Цитогенетические исследования
- Исследование состава камня
- Исследование клеща
- Прием гинеколога
- Срочные анализы
- Комплексные исследования
- Гематологические исследования
- Биохимические исследования
- Опухолевые маркеры
- Микроэлементы, витамины, аминокислоты
-
Иммунологические исследования
- Иммунный статус
-
Маркеры аутоиммунных заболеваний
- Диагностика аутоиммунного заболевания щитовидной железы
- Диагностика антифосфолипидного синдрома
- Диагностика системных заболеваний соединительной ткани
- Ревматоидный артрит, заболевания суставов
- Диагностика аутоиммунного поражения печени
- Васкулиты и поражения почек
- Диагностика аутоиммунного поражения желудочно-кишечного тракта
- Диагностика аутоиммунного заболевания кожи
- Диагностика заболевания сердца
- Проблемы репродуктивной системы
- Диагностика аутоиммунного заболевания поджелудочной железы
- Диагностика неврологических заболеваний
-
Диагностика аллергии
- Специфические IgE к пищевым аллергенам
- Специфические IgE к смеси аллергенов
- Специфические IgE к аллергенам пыльцы деревьев
- Специфические IgE к аллергенам сорных и луговых трав
- Специфические IgE к бытовым аллергенам
- Специфические IgE к эпидермальным аллергенам и белкам животного происхождения
- Специфические IgE к лекарственным аллергенам
- Специфические IgE к контактным аллергенам
- Специфические IgE к инсектным аллергенам
- Рекомбинантные аллергены
- Пищевая непереносимость
-
Гормональные исследования
- Лабораторная оценка функции щитовидной железы
- Лабораторная оценка состояния репродуктивной системы и мониторинг беременности
- Лабораторная оценка эндокринной функции почек и надпочечников
- Биогенные амины
- Лабораторная оценка эндокринной функции поджелудочной железы
- Гормон жировой ткани
- Эритропоэз
- Костный метаболизм
- Гормоны роста
- Функция эпифиза
- Оценка состояния желудочно-кишечного тракта
-
Диагностика инфекционных заболеваний
-
Вирусные инфекции
- Аденовирус, Ротавирус, Норовирус, Астровирус
- Варицелла-Зостер вирус (ветряная оспа, опоясывающий лишай)
- ВИЧ
- Герпес
- Гепатит А
- Гепатит В
- Гепатит Е
- Гепатит С
- Гепатит D
- Гепатит G
- Гепатит ТТV
- Грипп
- ОРВИ
- Коронавирус (COVID-19)
- Клещевой энцефалит
- Корь
- Краснуха
- Папилломавирусная инфекция
- Паротит эпидемический
- Респираторно-синцитиальный вирус
- Цитомегаловирус
- Энтеровирус
- Эпштейна-Барр вирус
-
Бактериальные инфекции
- Эрлихиоз, Анаплазмоз
- Дисбиотические состояния кишечника и урогенитального тракта
- Боррелиоз (болезнь Лайма)
- Бруцеллез
- Гарднерелла
- Гонорея
- Дифтерия
- Иерсиниоз
- Клостридиоз
- Коклюш, Паракоклюш, Бронхисептикоз
- Листериоз
- Микоплазменная инфекция
- Сальмонелла
- Сифилис
- Столбняк
- Стрептококковая инфекция
- Туберкулез
- Уреаплазменная инфекция
- Хеликобактерная инфекция
- Хламидийная инфекция
- Энтеробактерии, кампилобактерии
- Исследование на простейшие, паразиты, грибы
-
Вирусные инфекции
- Исследование кала
- Исследование мочи
- Цитологические исследования
- Гистологические исследования
- Бактериологические исследования
- Общие микроскопические исследования
-
Молекулярно - генетические исследования
- HLA-типирование генов
- Гематология
-
Моногенные заболевания
- Адреногенитальный синдром
- Акродерматит энтеропатический
- Альбинизм
- Анемия Даймонда-Блекфена
- Атрофия зрительного нерва
- Аутоиммунный лимфопролиферативный синдром
- Боковой амиотрофический склероз
- Велокардиофациальный синдром
- Вильсона-Коновалова болезнь
- Гемофилия
- Дефицит гормона гипофиза, комбинированный
- Миотония Томсена/Беккера
- Миотоническая дистрофия
- Муковисцидоз
- Мышечная дистрофия
- Нефротический синдром
- Остеопороз рецессивный (мраморная болезнь костей)
- Ретта синдром
- Фенилкетонурия
- Хорея Гентингтона (Болезнь Хангтингтона)
- Цистиноз нефропатический
- Эритрокератодермия
- Эритроцитоз рецессивный
- Риск развития онкологических заболеваний
- Определение биологического родства
- Носительство частых мутаций для наиболее частых наследственных заболеваний
- Бесплодие и невынашивание беременности, риск патологии плода
- Мультифакторные состояния
- Идентификация личности по ДНК
- Выделение ДНК из нестандартного образца
- Выделение ДНК при повторном предоставлении образца
- Судебная / досудебная экспертиза
- Комплексные генетические исследования
- Цитогенетические исследования
- Исследование состава камня
- Исследование клеща
- Прием гинеколога
Главная
/ Биохимические исследования
/ Диагностика нарушения обмена пуринов и пиримидинов
/ Обмен пуринов и пиримидинов в разовой моче (Урацил, Тимин, Гипоксантин, Ксантин, Дигидрооротовая кислота, Мочевая кислота, Дезокситимидин, Дезоксиуридин, Уридин, Дезоксиинозин, Дезоксигуанозин, Инозин, Гуанозин, Дигидроурацил, Дигидротимин, N-карбамил-бета-аланин, N-карбамил-бета-аминоизомасляная кислота) методом ВЭЖХ-МС
Обмен пуринов и пиримидинов в разовой моче (Урацил, Тимин, Гипоксантин, Ксантин, Дигидрооротовая кислота, Мочевая кислота, Дезокситимидин, Дезоксиуридин, Уридин, Дезоксиинозин, Дезоксигуанозин, Инозин, Гуанозин, Дигидроурацил, Дигидротимин, N-карбамил-бета-аланин, N-карбамил-бета-аминоизомасляная кислота) методом ВЭЖХ-МС
Метод исследования: ВЭЖХ-МС
Единицы измерения: мкмоль / ммоль креатинина
Врожденные (наследственные) болезни обмена пуринов и пиримидинов имеют широкий спектр клинических проявлений, которые включают среди прочего анемию, иммунодефицит, камни в почках, судороги, задержку психического развития, аутизм и задержку роста. В отличие от хорошо известных дефектов метаболизма пуринов большая часть из семи дефектов пиримидинового метаболизма описана совсем недавно. Наследственные нарушения обмена пуринов и пиримидинов – группа генетически обусловленных нарушений метаболизма, до сих пор мало изучались в Российской Федерации, несмотря на то что некоторые заболевания поддаются лечению. Во многом это обусловлено трудностями лабораторной диагностики данных заболеваний. С внедрением в лабораторную практику метода высокоэффективной жидкостной хроматографии-хроматомасс-спектрометрии (ВЭЖХ-МС) стала возможной диагностика большинства наследственных нарушений обмена.
Данное исследование представляет собой комплексный анализ концентрации азотистых оснований, нуклеозидов и их основных промежуточных и конечных метаболитов и предназначен для диагностики врождённых болезней обмена пуринов и пиримидинов.
Пурины и пиримидины являются абсолютно незаменимыми компонентами клеток: они необходимы для синтеза ДНК и РНК, запаса и транспорта энергии, синтеза ферментов, а также для передачи сигнала в клетку и его преобразования. Главными пуриновыми основаниями являются аденин и гуанин, пиримидиновыми – цитозин, тимин и урацил (Марри Р. и соавт., 1993). Указанные азотистые основания формируют основу структуры ДНК и РНК, а также ряда важнейших коферментов и циклических нуклеотидов. Поэтому поддержание баланса концентраций пуриновых и пиримидиновых оснований, нуклеозидов, нуклеотидов и их производных для каждого типа клеток или отдельных органов во многом определяет успешное развитие и функционирование как всего организма, так и определенных тканей и органов. Именно поэтому нарушения их обмена приводят к поражению сразу нескольких систем органов. Чаще эти нарушения обусловлены недостаточностью ферментов, необходимых для нормального метаболизма пуринов и пиримидинов, носят врождённый характер и проявляются в младенческом или раннем детском возрасте, хотя некоторые из них начинают проявляться только во взрослом возрасте. На сегодняшний день известно около 30 таких нарушений, 17 из которых приводят к заболеваниям.
Клиническая симптоматика наследственной патологии пуринового и пиримидинового обмена широко варьирует по степени тяжести даже среди родственников из одной семьи. Наиболее часто при данном нарушении метаболизма страдают центральная нервная система, почки и система крови (Simmonds H.A. et al., 1997). Основным биохимическим признаком этих заболеваний является изменение содержания пуриновых и пиримидиновых азотистых оснований, нуклеозидов и их производных в биологических жидкостях (Hartmann S. etal., 2006) и в лизатах клеток.
Преобладание в клинической картине признаков поражения той или иной системы организма позволяет выделить среди наследственных нарушений обмена пуринов и пиримидинов группы заболеваний в соответствии с ведущим симптомокомплексом.

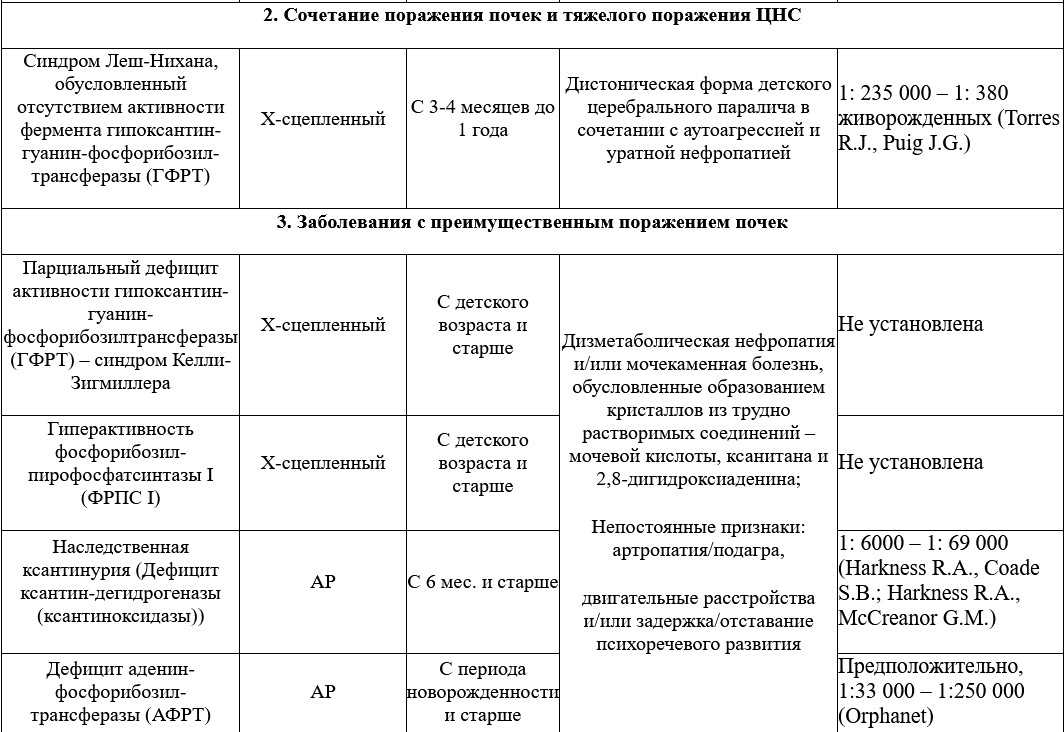
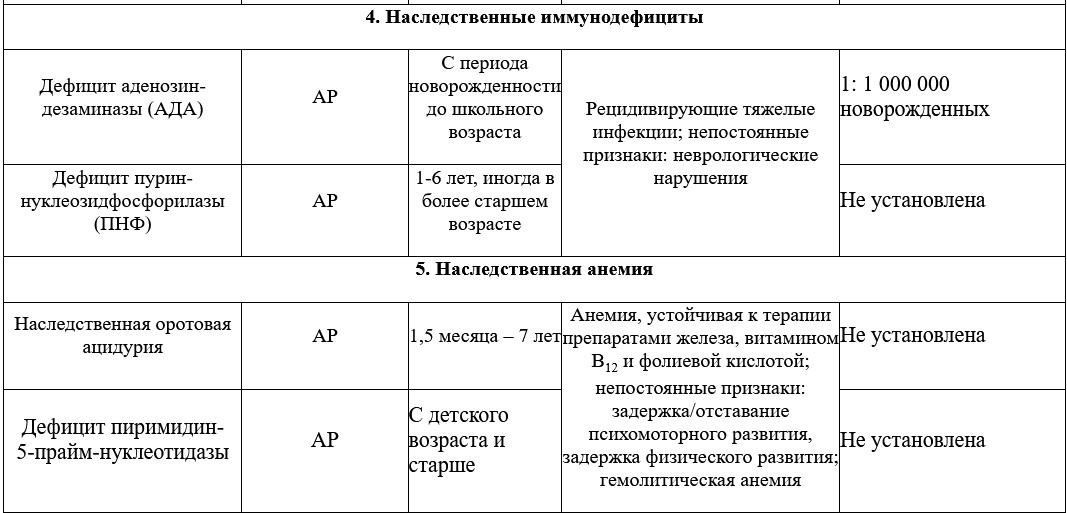
АР – аутосомно-рецессивный тип наследования;
АД – аутосомно-доминантный тип наследования.
Знание характерных клинических признаков позволяет выделить основные клинические показания для исследования обмена пуринов и пиримидинов:
Лабораторная диагностика наследственных нарушений обмена пуринов и пиримидинов включает «рутинные» и высокотехнологичные методы исследования. Ряд заболеваний, обусловленных нарушением обмена пуринов, можно заподозрить на основании изменения содержания мочевой кислоты в плазме крови и в моче, так как мочевая кислота является конечным продуктом катаболизма пуринов. Для установления диагноза большинства наследственных нарушений обмена пуринов и пиримидинов требуется исследование специфических метаболитов в биологических жидкостях (чаще всего в моче) или в клетках крови при помощи метода высокоэффективной жидкостной хроматографии-хроматомасс-спектрометрии (ВЭЖХ-МС). Данный метод является быстрым, точным и специфичным для диагностики нарушений этого вида обмена (Hartmann S. et al., 2006). ВЭЖХ-МС относится к высокотехнологичным методам исследования, требует специального оборудования и осуществляется в специализированных лабораториях и центрах, занимающихся наследственными болезнями обмена.
Показания к назначению:
Основными биохимическими показаниями для исследования нарушения обмена пуринов являются:
Основными клиническими показаниями являются:
Данное исследование проводится с целью:
Референсные значения (нмоль/мл) :
Уровень концентрации метаболитов пуринов и пиримидинов в моче зависит от пола, возраста, расовой принадлежности, особенностей питания, употребления алкоголя.



Результаты теста следует интерпретировать с учетом всех анамнестических, клинических и других лабораторных данных/
Причины повышения уровня Гуанозина, Инозина, Дезоксигуанозина - дефицит пурин-нуклеозид-фосфорилазы.
Причины повышения уровня Тимидина и Дезоксиуридина - дефицит тимидин-фосфорилазы
Причины повышения уровня мочевой кислоты - гиперактивность фосфорибозил-пирофосфат-синтетазы, дефицит гипоксантин-гуанин-фосфорибозил-трансферазы синдром Леша – Нихана, обусловленный отсутствием активности фермента гипоксантин-гуанин-фосфорибозил-трансферазы, гиперпродукция 5-фосфата,врождённое нарушение толерантности к фруктозе,болезнь накопления гликогена, болезнь Гоше, миело- и лимфопролиферативные заболевания, полицитемия, макроглобулинемия Валденстрема, гемолитическая анемия, избыточное поступление пуринов с пищей (мясо, пиво), гломерулонефрит, синдром Фанкони.
Причины понижения мочевой кислоты: дефицит фосфорибозил-пирофосфат-синтетазы, гиперактивность уридин-5-монофосфат-гидролазы, пурин-нуклеозид-фосфорилазы, ксантин-дегидрогеназы, ксантинурия, хронические заболевания почек (хронический гломерулонефрит), дефицит фолиевой кислоты, печеночная недостаточность, хронический алкоголизм, прием аллопуринола и его аналогов.
Причины повышения оротовой кислоты: дефицит фосфорибозил-пирофосфат-синтетазы, оротат-фосфорибозил-трансферазы, наследственная оротовая ацидурия
Причины повышения Бета-аланина: дефицит бета-аланин-альфа-кетоглутарат-аминотрансферазы
Причины повышения урацила: дефицит дигидропиримидин-дегидрогеназы, дигидропиримидиназы, бета-уреидопропионазы
Причины повышения Дезоксиаденозина: дефицит аденозин-дезаминазы (АДА)
Причины повышения ксантина: дефицит гипоксантин-гуанин-фосфорибозил-трансферазы, ксантин-дегидрогеназы, гиперактивность фосфорибозил-пирофосфат-синтазы I (ФРПС I), наследственная ксантинурия – дефицит ксантин-оксидоредуктазы (ксантиноксидазы)/
Вещества, которые могут увеличивать концентрацию мочевой кислоты: бета-адреноблокаторы, кофеин, витамин С, большие дозы ацетилсалициловой кислоты, кальцитриол, аспаргиназа, диклофенак, изониазид, ибупрофен, индометацин, пироксикам, парацетамол, соли лития, маннитол, меркаптопурин, метотрексат, нифедипин, преднизолон, верапамил.
Вещества, уменьшающие концентрацию мочевой кислоты в моче: аллопуринол, глюкокортикоиды, имуран, контрастные вещества, винбластин, азатиоприн, метотрексат, спиронолактон, инсулин, нестероидные противовоспалительные, мочегонные, пиразинамид, этамбутол, тетрациклин, циклоспорин.
Единицы измерения: мкмоль / ммоль креатинина
Врожденные (наследственные) болезни обмена пуринов и пиримидинов имеют широкий спектр клинических проявлений, которые включают среди прочего анемию, иммунодефицит, камни в почках, судороги, задержку психического развития, аутизм и задержку роста. В отличие от хорошо известных дефектов метаболизма пуринов большая часть из семи дефектов пиримидинового метаболизма описана совсем недавно. Наследственные нарушения обмена пуринов и пиримидинов – группа генетически обусловленных нарушений метаболизма, до сих пор мало изучались в Российской Федерации, несмотря на то что некоторые заболевания поддаются лечению. Во многом это обусловлено трудностями лабораторной диагностики данных заболеваний. С внедрением в лабораторную практику метода высокоэффективной жидкостной хроматографии-хроматомасс-спектрометрии (ВЭЖХ-МС) стала возможной диагностика большинства наследственных нарушений обмена.
Данное исследование представляет собой комплексный анализ концентрации азотистых оснований, нуклеозидов и их основных промежуточных и конечных метаболитов и предназначен для диагностики врождённых болезней обмена пуринов и пиримидинов.
Пурины и пиримидины являются абсолютно незаменимыми компонентами клеток: они необходимы для синтеза ДНК и РНК, запаса и транспорта энергии, синтеза ферментов, а также для передачи сигнала в клетку и его преобразования. Главными пуриновыми основаниями являются аденин и гуанин, пиримидиновыми – цитозин, тимин и урацил (Марри Р. и соавт., 1993). Указанные азотистые основания формируют основу структуры ДНК и РНК, а также ряда важнейших коферментов и циклических нуклеотидов. Поэтому поддержание баланса концентраций пуриновых и пиримидиновых оснований, нуклеозидов, нуклеотидов и их производных для каждого типа клеток или отдельных органов во многом определяет успешное развитие и функционирование как всего организма, так и определенных тканей и органов. Именно поэтому нарушения их обмена приводят к поражению сразу нескольких систем органов. Чаще эти нарушения обусловлены недостаточностью ферментов, необходимых для нормального метаболизма пуринов и пиримидинов, носят врождённый характер и проявляются в младенческом или раннем детском возрасте, хотя некоторые из них начинают проявляться только во взрослом возрасте. На сегодняшний день известно около 30 таких нарушений, 17 из которых приводят к заболеваниям.
Клиническая симптоматика наследственной патологии пуринового и пиримидинового обмена широко варьирует по степени тяжести даже среди родственников из одной семьи. Наиболее часто при данном нарушении метаболизма страдают центральная нервная система, почки и система крови (Simmonds H.A. et al., 1997). Основным биохимическим признаком этих заболеваний является изменение содержания пуриновых и пиримидиновых азотистых оснований, нуклеозидов и их производных в биологических жидкостях (Hartmann S. etal., 2006) и в лизатах клеток.
Преобладание в клинической картине признаков поражения той или иной системы организма позволяет выделить среди наследственных нарушений обмена пуринов и пиримидинов группы заболеваний в соответствии с ведущим симптомокомплексом.



АР – аутосомно-рецессивный тип наследования;
АД – аутосомно-доминантный тип наследования.
Знание характерных клинических признаков позволяет выделить основные клинические показания для исследования обмена пуринов и пиримидинов:
- Для болезней, протекающих с преимущественным поражением нервной системы, характерна задержка/отставание психического или психомоторного развития различной степени тяжести (от легкой до глубокой) с раннего возраста и часто сочетающаяся с мышечной гипотонией или гипертонусом, эпилептическими приступами, аутизмом.
- При заболеваниях с преимущественным поражением почек клиническая симптоматика обусловлена образованием в организме трудно растворимых соединений - мочевой кислоты, ксантина, 2,8-дигидроксиаденина, - что проявляется в виде дизметаболической нефропатии и/или мочекаменной болезни. Поражение почек часто сочетается с ранним развитием подагрического артрита и иногда – с неврологическими нарушениями в виде сенсоневральной тугоухости, атаксии, экстрапирамидных расстройств, задержки психомоторного развития; у отдельных больных возможно развитие острой почечной недостаточности.
- Сочетанное тяжелое поражение нервной системы и почек наблюдается при синдроме Леш-Нихана, обусловленном полным отсутствием активности фермента гипоксантин-гуанин-фосфорибозилтрансферазы (ГФРТ). Для заболевания характерна задержка психомоторного развития с 3-месячного возраста и формирование к 6 – 12 месяцам жизни дистонической формы церебрального паралича в сочетании с аутоагрессивным поведением и уратной нефропатией.
- Болезни, для которых характерна патология системы крови, проявляются либо в виде гипохромной анемии, устойчивой к терапии препаратами железа, витамином В12 и фолиевой кислотой, либо в виде гемолитической анемии. Анемия может сочетаться с задержкой/отставанием психомоторного развития и/или задержкой физического развития.
- Нарушения обмена пуринов, для которых характерна патология системы иммунитета, клинически манифестируют повторными утяжеляющимися с возрастом инфекциями (синуситами, отитами, трахеобронхитами и пневмониями), возможно фатальное течение вакцино-ассоциированной инфекции. У больных с иммунодефицитными состояниями нередко наблюдаются неврологические расстройства, включающие спастичность, нистагм, задержку психомоторного развития.
Лабораторная диагностика наследственных нарушений обмена пуринов и пиримидинов включает «рутинные» и высокотехнологичные методы исследования. Ряд заболеваний, обусловленных нарушением обмена пуринов, можно заподозрить на основании изменения содержания мочевой кислоты в плазме крови и в моче, так как мочевая кислота является конечным продуктом катаболизма пуринов. Для установления диагноза большинства наследственных нарушений обмена пуринов и пиримидинов требуется исследование специфических метаболитов в биологических жидкостях (чаще всего в моче) или в клетках крови при помощи метода высокоэффективной жидкостной хроматографии-хроматомасс-спектрометрии (ВЭЖХ-МС). Данный метод является быстрым, точным и специфичным для диагностики нарушений этого вида обмена (Hartmann S. et al., 2006). ВЭЖХ-МС относится к высокотехнологичным методам исследования, требует специального оборудования и осуществляется в специализированных лабораториях и центрах, занимающихся наследственными болезнями обмена.
Показания к назначению:
Основными биохимическими показаниями для исследования нарушения обмена пуринов являются:
- повышенное содержание мочевой кислоты в сыворотке крови в сочетании с повышенной экскрецией мочевой кислоты с мочой;
- низкое содержание мочевой кислоты в сыворотке крови в сочетании со снижением ее экскреции с мочой;
- снижение значения коэффициента суточной экскреции уратов с мочой по отношению к содержанию креатинина в суточном анализе мочи (Ur/Cr).
Основными клиническими показаниями являются:
- наличие признаков поражения нервной системы (врождённая глухота или слепота, задержка умственного развития, судороги, признаки аутизма, хореоатетоз)
- поражение суставов (подагрический артрит)
- поражение кроветворной системы (анемия, спленомегалия)
- поражение почек (нефролитиаз, кристаллурия)
Данное исследование проводится с целью:
- диагностики врождённых нарушений метаболизма пуринов и пиримидинов;
- мониторинга пациентов с нарушением обмена азотистых оснований;
- обследования родственников пациентов с нарушениями метаболизма пуринов и пиримидинов;
- оценки эффективности терапии;
Референсные значения (нмоль/мл) :
Уровень концентрации метаболитов пуринов и пиримидинов в моче зависит от пола, возраста, расовой принадлежности, особенностей питания, употребления алкоголя.



Результаты теста следует интерпретировать с учетом всех анамнестических, клинических и других лабораторных данных/
Причины повышения уровня Гуанозина, Инозина, Дезоксигуанозина - дефицит пурин-нуклеозид-фосфорилазы.
Причины повышения уровня Тимидина и Дезоксиуридина - дефицит тимидин-фосфорилазы
Причины повышения уровня мочевой кислоты - гиперактивность фосфорибозил-пирофосфат-синтетазы, дефицит гипоксантин-гуанин-фосфорибозил-трансферазы синдром Леша – Нихана, обусловленный отсутствием активности фермента гипоксантин-гуанин-фосфорибозил-трансферазы, гиперпродукция 5-фосфата,врождённое нарушение толерантности к фруктозе,болезнь накопления гликогена, болезнь Гоше, миело- и лимфопролиферативные заболевания, полицитемия, макроглобулинемия Валденстрема, гемолитическая анемия, избыточное поступление пуринов с пищей (мясо, пиво), гломерулонефрит, синдром Фанкони.
Причины понижения мочевой кислоты: дефицит фосфорибозил-пирофосфат-синтетазы, гиперактивность уридин-5-монофосфат-гидролазы, пурин-нуклеозид-фосфорилазы, ксантин-дегидрогеназы, ксантинурия, хронические заболевания почек (хронический гломерулонефрит), дефицит фолиевой кислоты, печеночная недостаточность, хронический алкоголизм, прием аллопуринола и его аналогов.
Причины повышения оротовой кислоты: дефицит фосфорибозил-пирофосфат-синтетазы, оротат-фосфорибозил-трансферазы, наследственная оротовая ацидурия
Причины повышения Бета-аланина: дефицит бета-аланин-альфа-кетоглутарат-аминотрансферазы
Причины повышения урацила: дефицит дигидропиримидин-дегидрогеназы, дигидропиримидиназы, бета-уреидопропионазы
Причины повышения Дезоксиаденозина: дефицит аденозин-дезаминазы (АДА)
Причины повышения ксантина: дефицит гипоксантин-гуанин-фосфорибозил-трансферазы, ксантин-дегидрогеназы, гиперактивность фосфорибозил-пирофосфат-синтазы I (ФРПС I), наследственная ксантинурия – дефицит ксантин-оксидоредуктазы (ксантиноксидазы)/
Вещества, которые могут увеличивать концентрацию мочевой кислоты: бета-адреноблокаторы, кофеин, витамин С, большие дозы ацетилсалициловой кислоты, кальцитриол, аспаргиназа, диклофенак, изониазид, ибупрофен, индометацин, пироксикам, парацетамол, соли лития, маннитол, меркаптопурин, метотрексат, нифедипин, преднизолон, верапамил.
Вещества, уменьшающие концентрацию мочевой кислоты в моче: аллопуринол, глюкокортикоиды, имуран, контрастные вещества, винбластин, азатиоприн, метотрексат, спиронолактон, инсулин, нестероидные противовоспалительные, мочегонные, пиразинамид, этамбутол, тетрациклин, циклоспорин.
Исключить (по согласованию с врачом) прием мочегонных препаратов в течение 48 часов до сбора мочи.
Срок выполнения с момента поступления в лабораторию:
3-10 дней
Тип биоматериала
разовая порция мочи
Цена услуги
7600 руб
Процедура взятия биоматериала оплачивается отдельно и зависит от типа материала:
Взятие крови из периферической вены
150 руб
Взятие биоматериала в процедурном кабинете (отделяемое мочеполовых органов)
230 руб
Взятие биоматериала в процедурном кабинете (отделяемое уха, глаза, верхних дыхательных путей)
120 руб
Взятие биоматериала на коронавирус (соскоб из ротоглотки, соскоб из носоглотки)
160 руб
Клиентам
Анализы и цены
Как сдать анализы
Вызов на дом
Семейный доступ
Справка для ФНС
Политика обработки персональных данных
Договор на оказание платных медицинских
услуг
Для граждан с ограниченными возможностями
Способы оплаты
Телефоны вышестоящих организаций
Пересчёт единиц измерения
Позвоните, если остались вопросы

Используя сайт gemohelp.ru, вы соглашаетесь с использованием файлов cookie и обработкой Ваших персональных данных с помощью сервиса "Яндекс.Метрика".